Phương pháp sàng lọc trước sinh mới nhất hiện nay, có độ chính xác cao và không xâm lấn, được thực hiện dựa trên việc phân tích adn của thai nhi có trong máu của người mẹ. Phương pháp này có thể được thực hiện vào cuối giai đoạn thứ nhất của thai kỳ và đạt tỷ lệ chính xác cao so với các phương pháp truyền thống.>>
dịch vụ xét nghiệm ADN huyết thống
Chia sẻ cách thức mới xét nghiệm thai nhi
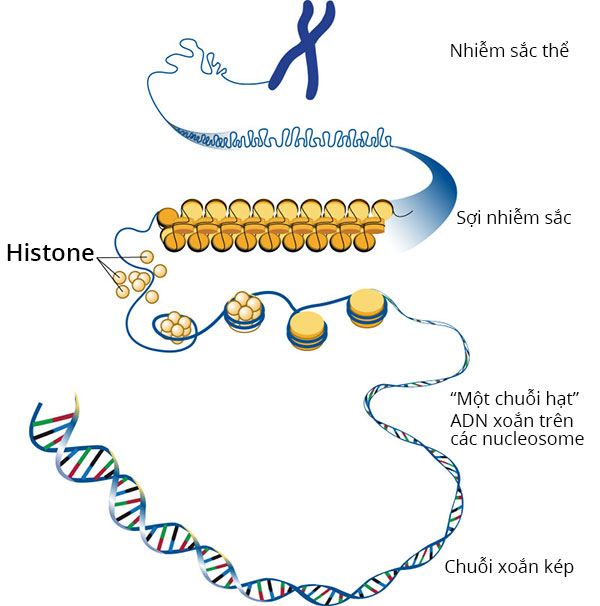
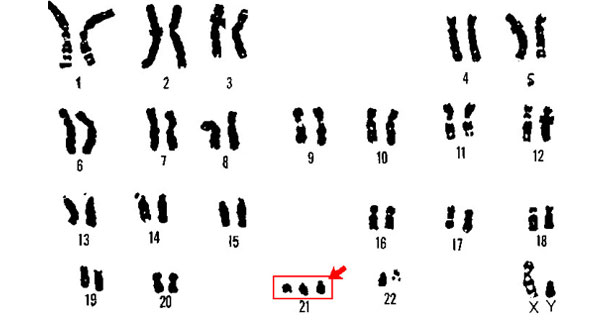
Theo thống kê vào năm 2005 của Bộ Y tế, tại Việt Nam số người mắc các dị tật bẩm sinh và bất thường về nhiễm sắc thể chiếm 0,26% trên tổng số bệnh nhân tại các bệnh viện . Hàng năm ở nước ta có khoảng 20.000 trường hợp trẻ có dị tật bẩm sinh và bất thường về nhiễm sắc thể gây ra Hội chứng Down được sinh ra, nhưng trên thực tế trong cộng đồng, con số này có thể lớn hơn rất nhiều. Việc phát hiện sớm các bất thường nhiễm sắc thể là việc cần thiết để người mẹ có nhiều lựa chọn cho thai nhi trong bụng.
Báo The New York Times và Discover đã có bài giới thiệu về phương pháp xét nghiệm trước sinh không xâm lấn với nhiều ưu điểm như có thể phát hiện sớm các bất thường nhiễm sắc thể từ tuần lễ thứ 10 của thai kỳ, và an toàn với thai nhi hơn so với phương pháp chọc ối truyền thống.
Chẩn đoán trước sinh
Hơn 30 năm trước, một người bạn của tôi đã có thai ngoài ý muốn ở tuổi 37, bác sỹ sản khoa khuyên không nên làm xét nghiệm thai nhi bằng phương pháp chọc ối vì “quá nguy hiểm” và có nguy cơ sẩy thai. Cuối cùng, cháu bé ra đời và bị ảnh hưởng trầm trọng bởi hội chứng Down, vốn có thể dễ dàng phát hiện được nếu trước đó cô ấy làm xét nghiệm trước sinh.
Với nền y học hiện nay thì câu chuyện của bạn tôi sẽ có một hồi kết khác. Cô ấy sẽ trải qua một loạt các xét nghiệm sàng lọc, và nếu kết quả cho thấy có nguy cơ cao mắc hội chứng Down thì phương pháp xét nghiệm thai xâm lấn thông qua chọc ối (amniocentesis) sẽ được thực hiện. Cô ấy sẽ có quyền lựa chọn bỏ hay giữ cái thai.
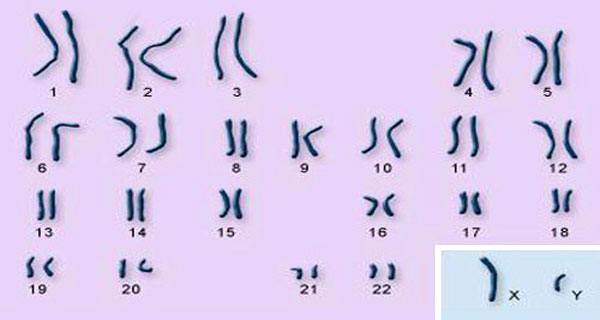
Xét nghiệm thai nhi bằng phương pháp không xâm lấn có thể phát hiện sớm Hội chứng Down. Ảnh: The New York Times
Trong tương lai, nếu một sản phụ quyết định giữ lại thai có dấu hiệu của hội chứng Down, cô ta sẽ được đề nghị thực hiện các biện pháp điều trị trước sinh nhằm làm giảm sự phát triển của những tác nhân tiêu cực lên thai.
Chẩn đoán trước sinh đã đạt được bước tiến lớn kể từ giữa thập niên 70 và hiện tại đang trên đỉnh cao của những phát triển mang tính cách mạng, góp phần làm cho việc chẩn đoán thai là một phần không thể thiếu của quá trình chăm sóc sức khỏe sinh sản.
Phương pháp sàng lọc mới
Gần bốn thập kỷ kể từ khi phương pháp chọc ối được công nhận rộng rãi, các kỹ thuật mới không ngừng đạt được những tiến bộ trong việc nâng cao độ chính xác và an toàn cho các chẩn đoán trước sinh. Người ta đã phát triển phương pháp xét nghiệm thai nhi có thể phát hiện được hơn 800 rối loạn gen và số thai phụ phải thực hiện chọc ối hay CVS (chorionic villus sampling) giảm đi đáng kể.
Phương pháp sàng lọc mới nhất hiện nay, có độ chính xác cao và không xâm lấn, được thực hiện dựa trên việc phân tích ADN của thai nhi có trong máu của người mẹ. Theo nghiên cứu ở một số quốc gia, phương pháp này khá chính xác trong việc phát hiện hội chứng Down ở một vài trường hợp đã bị bỏ sót và từ đó giúp giảm thiểu số thai phụ phải làm xét nghiệm xâm lấn để xác định hay loại bỏ sự hiện diện của Down.
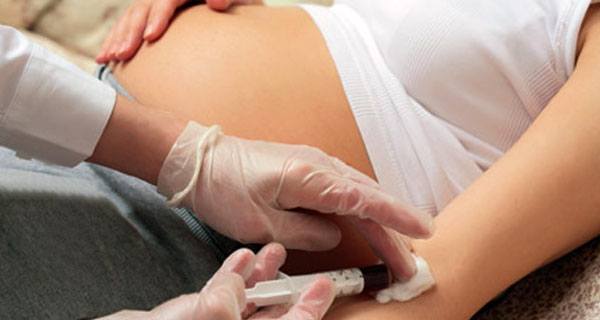
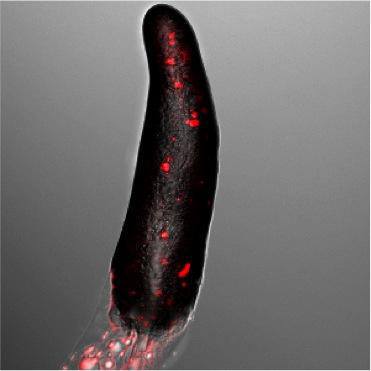
Xét nghiệm trước sinh không xâm lấn bằng cách phân tích ADN của thai nhi có trong máu người mẹ. Ảnh: ostetriciaeginecologia.sm
Xét nghiệm mới này được thực hiện vào cuối giai đoạn 1 của thai kỳ, có thể phát hiện thêm các bệnh về gen khác, ví dụ như có thêm các bản sao của nhiễm sắc thể 13 và 18, hay mất đi một nhiễm sắc thể giới tính. Tuy nhiên hiện nay Cục quản lý thực phẩm và dược phẩm Hoa Kỳ (FDA) vẫn chưa phê duyệt loại xét nghiệm mới này, và Trường Cao đẳng Sản và phụ khoa Hoa Kỳ đề xuất chỉ nên áp dụng cho các trường hợp có nguy cơ cao mắc các chứng bất thường nhiễm sắc thể.
Theo Tiến sỹ Diana W. Bianchi, nhà nghiên cứu nhi khoa và gen đến từ Đại học Dược Tufts, phần lớn các thai phụ đều có thể thực hiện phương pháp sàng lọc mới này nếu có yêu cầu của bác sĩ và họ tự nguyện trả các chi phí phát sinh. Tiến sỹ Bianchi, hiện nay đang tham gia trong ban cố vấn cho một công ty thực hiện các xét nghiệm ADN thai nhi, cho biết bà kỳ vọng các xét nghiệm này sẽ sớm nằm trong danh sách thực hiện cho tất cả các phụ nữ có thai bởi vì ngoài “sự chính xác lạ thường” khi phát hiện hội chứng Down ở thai nhi, chúng có thể được thực hiện sớm hơn các phương pháp khác và từ đó giảm thiểu chi phí cũng như nguy cơ xảy ra biến chứng.
Thực nghiệm khoa học
Tại Mỹ, cứ 700 trẻ em ra đời thì có 1 trường hợp mắc hội chứng Down, đây được xem là chứng bất thường nhiễm sắc thể phổ biến nhất cho đến thời điểm hiện nay. Nó gây ảnh hưởng cả về thể lực và trí lực đủ mức độ từ nhẹ đến nặng.
Trong quá khứ, quyết định thực hiện xét nghiệm nước ối hay C.V.S được dựa trên tuổi của thai phụ hay quá trình theo dõi về gen. Phụ nữ tuổi càng cao, thì càng có nguy cơ sinh con có khiếm khuyết về gen do một số bất thường về nhiễm sắc thể.>>
Giám định ADN hành chính
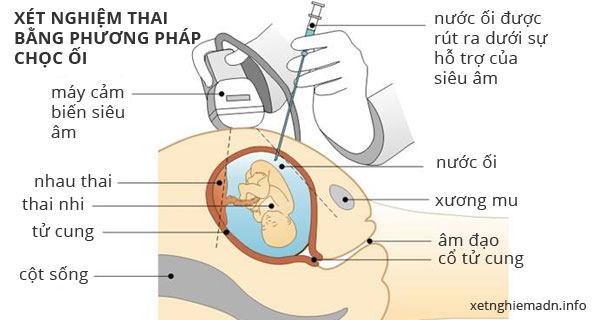
Xét nghiệm thai nhi xâm lấn bằng phương pháp chọc ối.
Theo tiêu chuẩn hiện nay, tất cả phụ nữ có thai sẽ được đề nghị thực hiện một loạt các xét nghiệm sàng lọc (prenatal diagnosis) không xâm lấn vào giai đoạn thứ nhất và thứ hai của thai kỳ nhằm phát hiện hiện khả năng bào thai có thêm một nhiễm sắc thể số 21, vốn là nguyên nhân gây ra Hội chứng Down. Sau đó thai phụ sẽ quyết định việc thực hiện chọc ối (hoặc CVS) hay không.
Gộp chung lại thì các phương pháp sàng lọc truyền thống có thể phát hiện 92% các ca mắc Hội chứng Down, nhưng lại bỏ qua 8% còn lại. Tiếp đó, trong các kết quả kết luận dương tính với Down, có 5% không chính xác.
Phương pháp chọc ối được thực hiện vào tuần thứ 15 đến 20 của thai kỳ, bao gồm đưa một mũi kim dài vào bọc ối của người mẹ, sau đó hút ra một lượng nước ối và tế bào bao quanh thai nhi. Ở phương pháp CVS, người ta thường làm tại tuần thứ 11 của thai kỳ, bằng cách lấy mẫu tế bào thai nhi từ nhau thai. Các tế bào sau đó được phân tích để kiểm tra các khiếm khuyết về gen. Cả hai cách làm này đều có một xác suất nhỏ dẫn đến sẩy thai.
Phương pháp chẩn đoán mới bằng cách phân tích ADN của thai có trong máu của người mẹ có thể phát hiện hầu như toàn bộ các trường hợp mắc hội chứng Down, và trong số đó chỉ có ít hơn 1% báo dương tính giả. Chỉ những trường hợp có kết quả dương tính mới cần phải thực hiện chọc ối hay CVS để kết luận sự hiện diện của hội chứng Down, và chỉ có 1 trong số 1000 phụ nữ đã được chẩn đoán bằng phương pháp mới cần phải tiếp tục tiến hành phương pháp xâm lấn để xác định rõ bào thai của cô ấy không có hội chứng Down.
Hướng phát triển tương lai
Trong một bài báo đăng trên Tạp chí y học New England, Stephanie Morain, nghiên cứu sinh tại Đại học Harvard, cùng với đồng tác giả cho rằng phương pháp xét nghiệm ADN thai nhi có một số hạn chế nhất định. Một số hội chứng bất thường nhiễm sắc thể vẫn bị bỏ sót nếu so sánh với phương pháp sàng lọc truyền thống, và “phương pháp mới này chưa được ngành bảo hiểm áp dụng rộng rãi”. Chi phí cho các xét nghiệm khoảng từ $800 đến hơn $2000, mặc dù một số công ty đưa ra “giá giới thiệu” đặc biệt chỉ vào khoảng $200.
Phương pháp mới này không được yêu cầu phải tuân theo các tiêu chuẩn ngặt nghèo về an toàn và hiệu quả ban hành bởi FDA, và chỉ có thể áp dụng cho các ca sinh đơn. Hàng chục ngàn xét nghiệm đã được thực hiện cho đến thời điểm hiện nay.
Người ta chỉ cần lấy một ít mẫu máu của người mẹ, trong đó có chứa ADN của cô ta và cả thai nhi. Trong một lần phỏng vấn, tiến sỹ Bianchi đã chia sẻ rằng tại tuần lễ thứ 10 của thai kỳ, trung bình chỉ có khoảng 10-12% ADN trong máu của người mẹ là ADN của bào thai.
Sử dụng các kỹ thuật giải trình tự gen tiên tiến, người ta sẽ phân tích ADN nhanh chóng chỉ với một chi phí tương đối thấp, bởi vì một lần thực hiện có thể phân tích đồng thời mẫu của nhiều người. Tiến sỹ Lee P. Shulman, nhà di truyền học tại Đại học dược Northwestern Feinberg, nhấn mạnh rằng phương pháp xét nghiệm ADN mới này cũng giống như các phương thức sàng lọc khác, không thực sự là “chẩn đoán” đúng nghĩa, một kết quả dương tính cần phải được xác nhận bởi một xét nghiệm nước ối hay CVS.